서 론
연반증(malakoplakia)은 흔치 않은 만성 육아종성 염증 질환으로 악성 종양, 자가 면역 질환, 면역 결핍 질환, 만성 알코올 남용, 조절되지 않는 당뇨 또는 장기간 스테로이드나 면역 억제제를 복용 중인 환자 등 주로 면역 기능이 저하된 환자에서 발병하는 것으로 알려져 있다[1]. 연반증은 다양한 신체 부위에서 발생할 수 있으나 주로 비뇨생식계, 특히 방광 및 요도를 잘 침범하며 신 실질 침범은 비교적 적어 약 15%에서 발생하는 것으로 보고되고 있다. 신 실질 연반증은 현재까지 국내에서 약 10예가 보고되었으며 이 중에서 급성 신손상이 동반된 사례는 한 예에 불과하였으며, 급성 간질성 신염에 의한 급성 신손상과 동반된 증례는 보고된 바가 없다[2,3]. 최근 저자들은 간질성 신염에 의한 급성 신손상으로 내원한 80세 여자 환자에서 신 실질 연반증이 동반되어 치료한 증례를 경험하였기에 이를 문헌 고찰과 함께 보고하는 바이다.
증 례
환자는 80세 여자 환자로 수년 전부터 고혈압으로 hydrochlorothiazide 25 mg를 복용 중이었으며 파킨슨병으로 carbidopa 25 mg/levodopa 100 mg, escitalopram oxalate 10 mg, rivastigmine 4.6 mg/24 hr 투약을 유지 중이었다. 이 외에 당뇨, 결핵, 간염 등의 병력은 없었다. 환자는 내원 1달 전부터 성분을 알 수 없는 각종 농축액 및 약제를 구입하여 복용해 오던 중 내원 5일 전부터 발생한 의식저하, 오심, 구토, 전신 쇠약감으로 내원하였다. 내원 당시 혈압 115/65 mmHg, 맥박 분당 99회, 호흡수 분당 15회, 체온 36.0°C였다. 전신 소견에서 만성 병색을 보였고 의식은 졸린 모습을 보였다. 결막은 창백하지 않았고, 공막의 황달 소견은 없었으며 흉부 청진에서 심음 및 호흡음은 정상이었다. 복부는 부드러웠고 장음은 증가되어 있지 않았으며 압통 및 반발통은 없었다. 하지 부종은 관찰되지 않았고, 늑골 척추각 압통은 없었다.
일반 혈액검사에서 혈색소 11.4 g/dL, 혈소판 400,000/μL, 백혈구 13,950/μL (중성구 88.7%, 림프구 6.3%, 단핵구 3.0%, 호산구 0.5%)였다. 혈청 생화학 검사에서 혈액요소질소 >200 mg/dL, 크레아티닌 8.38 mg/dL로 상승 소견 보였으며 추정 사구체 여과율은 5 mM/min/1.73 m2으로 감소되어 있었고 혈청 전해질 농도는 Na 150 mmol/L, K 3.8 mmol/L, Cl 113 mmol/L, tCO2 13 mmol/L이었으며 혈청 삼투질 농도는 393 mOsm/kg로 증가되어 있었다. 간기능 및 응고 검사는 정상 범위였다. 소변 검사에서는 요비중 1.013, pH 5.0, 요단백 (1+), 백혈구 (3+), 적혈구 (3+), 아질산염 양성 소견을 보였고 고배율 시야에서 다수의 백혈구 및 10~20개의 적혈구가 관찰되었다. 혈청 면역단백 중 C3는 79.1 mg/dL (90~180 mg/dL), C4 41.30 mg/dL (10~40 mg/dL)이었고, CRP (C-reactive protein)는 26.6 mg/L로 상승 되어 있었다. 혈청 IgG/IgA/IgM은 각각 1,814/534/86 mg/dL (700~1,600/70~400/40~230 mg/dL) 이었다. 단회뇨의 단백/크레아티닌 비율은 2.20 g/gCr였다.
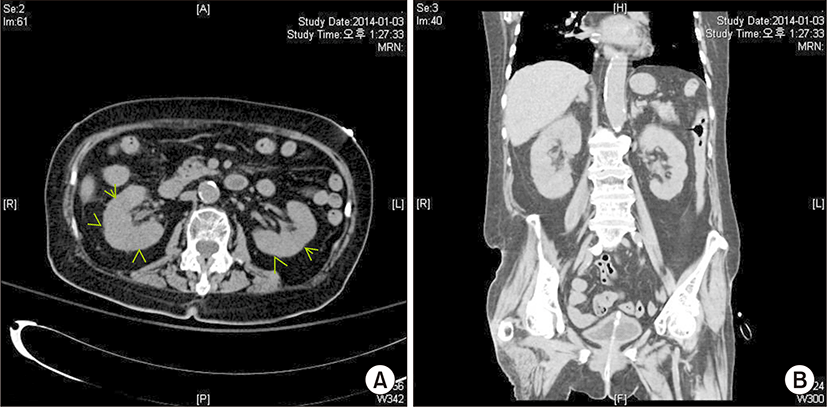
흉부 방사선 촬영은 정상 소견을 보였으며 복부 전산화 단층 촬영에서 림프절 종대 및 복수의 소견은 없었으며, 수신증의 소견은 없었다. 우측 신장의 장축은 10.5 cm, 좌측 신장은 9.7 cm으로 정상 범위였으나, 양측 신장에 쐐기 모양의 감쇠 차이를 보이는 다발성 병변이 관찰되었다(Fig. 1).
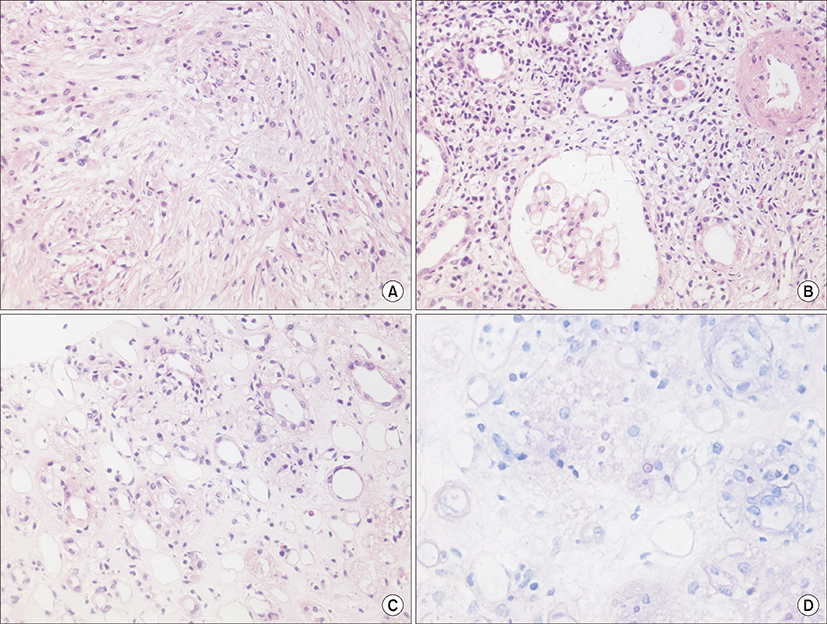
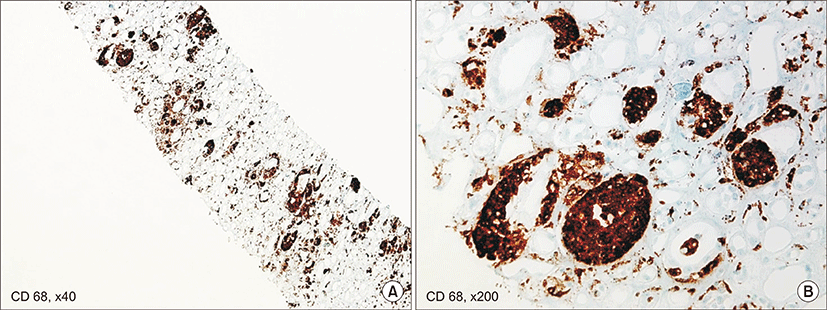
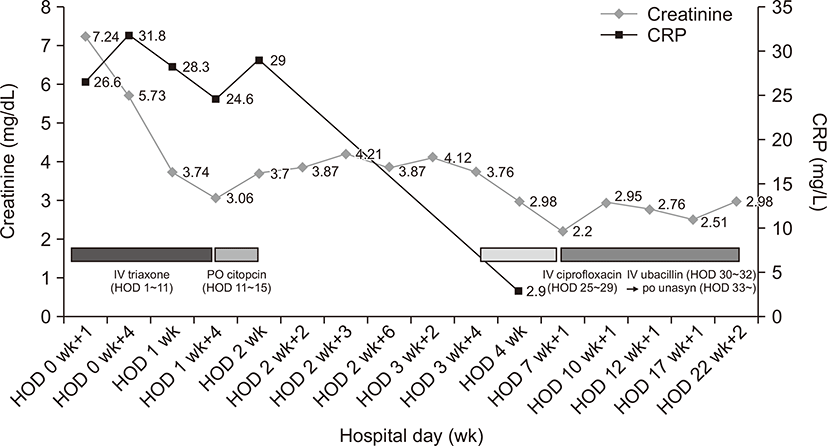
정맥 수액요법과 요로감염에 대해 경험적으로 항생제 투여를 시작하였다. 요 세균배양 검사에서 extended spectrum beta-lactamase (-) Escherichia coli 동정되어 ceftriaxone을 정주로 유지하였다. 보존적 치료 후 크레아티닌이 3.03 mg/dL까지 호전되었다가 다시 4.21 mg/dL로 상승하여 정확한 급성 신손상의 원인을 확인하기 위하여 신조직 검사를 시행하였다. 조직검사에서 부분적인 섬유화 및 형질 세포 침윤을 동반한 급성 및 만성 간질성 신염 소견을 보였다(Fig. 2A-C). 신장 조직에 대한 추가검사로 CD68 및 CK7에 대한 염색이 실시되었고, 원위 세뇨관 및 집합 세관 주변으로 다수의 CD68 양성 세포들이 관찰되었으며 일부에서는 세뇨관에서도 CD68및 CK7 양성 세포들이 관찰되어 염증성 병변에 대한 대식세포 침윤으로 판단되었다(Fig. 3). 아울러 Periodic acid-Schiff (PAS) 염색 양성의 둥근 과립이 간질 및 세관 내에서 관찰되어 Michaelis-Gutmann body로 판단하였으며 따라서 섬유화를 동반한 병변을 포함하여 모두 연반증에 합당한 소견이었다(Fig. 2D). 신 실질 연반증 진단 후 항생제를 ciprofloxacin으로 지속 투여하였으며, 요 세균배양 검사 상 Enterococcus faecalis 동정되어 항생제를 ubacillin으로 교체하였다. 이후 크레아티닌 2.55 mg/dL까지 감소하여 경구 항생제를 유지하여 퇴원 후 현재 4달째 경구 항생제를 유지하며(unasyn, 375 mg three times a day), 크레아티닌 2.5 mg/dL로 안정적인 상태로 경과 관찰 중이다(Fig. 4).
고 찰
연반증은 1902년 Michaelis와 Gutmann에 의해 처음으로 기술된 만성 육아종성 염증 질환으로 주로 요로감염의 과거력이 있는 중년 여성에서 호발하며 coliform bacteria가 주요 원인균으로 이중 70~75%가 E. coli에 의한 것으로 알려져 있다. 연반증은 세포내의 cGMP (cyclic guanosine monophosphate) 농도 감소로 인해 단핵구의 포식용해소체(phagolysosome) 기능 장애가 발생하여 발병하는 것으로 알려져 있으며 불완전하게 식균된 세균의 침착은 석회화된, PAS 염색 양성의 호염기성 봉입체를 형성하게 되는데 이것이 연반증의 특징적인 Michaelis-Gutmann body이며 연반증의 진단은 조직병리학적으로 Michaelis-Gutmann body를 확인함으로써 확진할 수 있다[3,4].
연반증은 비뇨생식기계 뿐만 아니라 소화기계, 후복강, 피부, 폐, 뇌 등 다양한 장기를 침범하는 것으로 알려져 있으며 침범 장기에 따라 다양한 임상 증상을 나타낸다[2]. 신 실질 연반증의 경우 발열, 종괴의 촉지, 다뇨, 빈뇨, 복통, 측와부 통증 등의 임상 증상을 나타내며 검사상 빈혈, 백혈구 증가증, 농뇨, 단백뇨, 혈뇨가 동반된다[4]. 발현 당시 신부전이 동반되는 경우에 신부전의 정도는 다양한 것으로 보고되고 있다[5]. 영상학적 소견 또한 연반증의 단계에 따라 전반적인 신비대 에서부터 단발성 혹은 다발성의 결절, 신장주위 침범을 동반한 신농양, 다발성의 결절을 동반한 신위축까지 다양하게 나타난다. 대부분 신 비대 소견을 보이며 신 실질 내의 단발성 또는 다발성 침윤이 가성 종양(pseudo-tumor)의 양상을 띠기도 하여 신종양으로 오인되는 경우도 많다[3].
신 실질 연반증의 치료로 이전에는 수술적 치료가 많이 시행되었으나 fluoroquinolone의 사용으로 신 실질 연반증의 완치가 가능하다는 것이 밝혀지면서, 1990년대 이후로 세포내부로의 침투가 우수한 trimethoprim/sulfamethoxazole, rifampin, fluoroquinolone 등의 항생제를 장기간 사용하는 내과적 치료가 우선적으로 고려되고 있다. 또한, 이와 더불어 bethanecol 및 ascorbic acid 등도 세포내의 cGMP 농도를 증가시키는 것으로 알려져 있어 항생제와 함께 투여되기도 한다.
본 증례를 포함하여 현재까지 국내에서 보고된 증례들을 분석해 보았을 때(Table 1) [1,2,6-11] 평균 발생 연령은 61.8세, 열 명 중 일곱 명이 여성으로 여성에서 호발하는 경향을 보였다. 평균 혈색소 9.8 mg/dL, 백혈구 18,290/μL으로 빈혈 및 백혈구 증가증이 동반되어 있었고 75%에서 농뇨가 확인되었다. 약 44%에서 원인균이 확인되었으며 이 중 E. coli가 75%를 차지하였다. 발현 양상의 경우 간, 폐, 신장 주변 조직 등을 침범하는 종괴 양상으로 나타나는 경우가 가장 많았으며(60%), 신부전으로 발현된 경우가 30%, 단백뇨로 발현된 경우가 10%를 차지하였다. 급성 신부전으로 발현된 예는 본 증례를 포함하여 총 2예였으며 급성 간질성 신염으로 발현된 경우는 본 증례가 처음이었다. Jung 등[8]의 증례에서는 급성 신부전에 대해 일시적인 신대체 요법이 시행되었으며 충분한 항생제 사용에도 임상증상 호전 보이지 않아 스테로이드 충격요법 시행되었고 이후 부분적인 신기능 회복을 보여 신대체 요법을 중단하였다. 국외 문헌을 고찰해보면, 신 실질 연반증 사례들을 분석한 Tam 등[12]의 보고서에 따르면 25예 중 6예(24%)에서 신부전이 동반되었으며 이중 3예에서 신대체 요법을 필요로 하였는데 2예에서는 신 실질 연반증 진단 후 3년까지는 부분적인 신기능 회복을 보이다가 이후에 신부전으로 진행된 경우였다. 이는 간질성 신염이 신 실질 연반증에 선행하며 연반증이 진행될 경우 간질성 섬유화가 발생한다는 가설을 뒷받침한다고 할 수 있겠다. 또한 간질이 결정적 시점을 지나 파괴될 경우 항생제 치료를 지속한다 하더라도 불가역적 신손상이 발생할 수 있다는 사실을 보여주는 결과라 하겠다.
신 실질 연반증은 높은 사망률(~70%) 및 낮은 신기능 회복률(~10%)과 연관되어 있었으나 세포내부로의 침투가 우수한 trimethoprim/sulfamethoxazole, fluoroquinolone과 같은 항생제가 도입되면서 생존율이 향상되었으며 국내 사례들을 분석한 결과에서도 연반증으로 인해 사망한 사례는 없었다[12].
신 실질 연반증은 발생빈도가 낮고 발현 양상이 다양하여 임상적으로 의심하기가 어려운 질환이다. 연반증에 대한 적절한 치료가 지연될 경우 간질성 섬유화로 인해 만성 신부전으로 진행될 가능성이 증가하므로 조기 진단 및 치료가 중요하다. 국내외사례들을 분석해 보았을 때 신 실질 연반증에서 발현 당시 신부전이 동반되는 경우가 적지 않으므로 요로 감염이 동반되어 있거나 이전 요로감염의 과거력이 있으며 신부전의 원인이 명확하지 않을 경우 신 실질 연반증을 고려하여 진단을 위해 복부 전산화 단층 촬영 및 신장 조직검사 등을 시행하고 이를 토대로 적절한 항생제 치료가 이루어져야 할 것이다.