서 론
소세포 폐암은 전체 암 발생 중 1~2%를 차지한다. 치료를 하지 않을 경우 생존기간이 2~3개월 정도로 짧지만 화학요법의 반응률이 50~85%로 높아, 적극적인 화학요법이 생존기간 연장에 도움이 되는 것으로 알려져 있다. 한편, 투석환자에서의 화학요법은 독성 증가의 우려 등으로 인해 적극적으로 진행되지 못하는 경향이 있으며, 현재까지 이에 대한 적절한 임상 시험이 존재하지 않고, 각 암 종 별로 수 건의 증례보고만 있는 실정이다. 저자들은 혈액 투석 중인 소세포 폐암 환자에서 carboplatin과 irinotecan, carboplatin과 etoposide, 그리고 cisplatin과 irinotecan을 사용한 화학요법을 시행하여 심각한 독성 없이 임상적 반응을 확인한 2건의 증례를 보고한다.
증 례
65세 남자가 흉부 단순 촬영에서 이상 소견이 보여 추가적인 검사와 치료를 위해 내원하였다. 환자는 44갑년의 흡연력이 있었으며 35년 전 당뇨병으로 진단받아 인슐린을 사용 중이었고, 8년 전 고혈압으로 진단받아 경구 약제를 복용 중이었다. 당뇨병에 의한 만성 신부전으로 투석 치료를 하던 중, 흉부 단순촬영에서 이상 소견이 확인되었다. 이에 타 병원에서 흉부 컴퓨터 단층촬영(computed tomography, CT), 기관지 내시경, 내시경적 생검 진행 후, 최종적으로 우중엽 기관지 입구에 위치한 소세포 폐암으로 진단되어 본원에 의뢰되었다.
검진 시 좌측 팔의 동정맥루 외에 환자의 활력 징후와 신체 검진에서 특이 소견은 없었다. 혈액검사에서 백혈구 6,390/μL, 혈색소 9.5 g/dL, 혈소판 189,000/μL, 일반 화학검사에서 Na/K/Cl 136/4.0/95 mmol/L, Ca/P 8.7/5.6 mg/dL, BUN/Cr 60/5.1 mg/dL, AST/ALT 25/14 IU/L, total bilirubin 0.3 mg/dL, ALP 62 IU/L이 확인되었다. 양전자 단층촬영(positron emission tomography, PET) (Fig. 1A)에서 우하엽, 종격동 림프절(5, 7, 10R), 그리고 좌측 치골의 과대사 부위가 관찰되어 악성 림프절 종대 및 골전이가 확인되었다.
확장기 소세포 폐암으로 진단, carboplatin (5 area under curve [AUC], 1일)과 irinotecan (50 mg/m2, 1일, 8일)을 이용한 화학요법을 3주 간격으로 시행하기로 하였다. 화학요법 당일, 항암제 주입이 끝난 후 한 시간 뒤에 혈액 투석을 시행하였고, 이후로는 주 3회(2일 또는 3일에 1회)로 혈액투석을 시행하였다. 주 3회 투석일정과 항암제 투여 일정이 맞지 않을 경우, 투석일정을 조절하여 항암제를 투여한 날에 투석을 진행하도록 하였다.
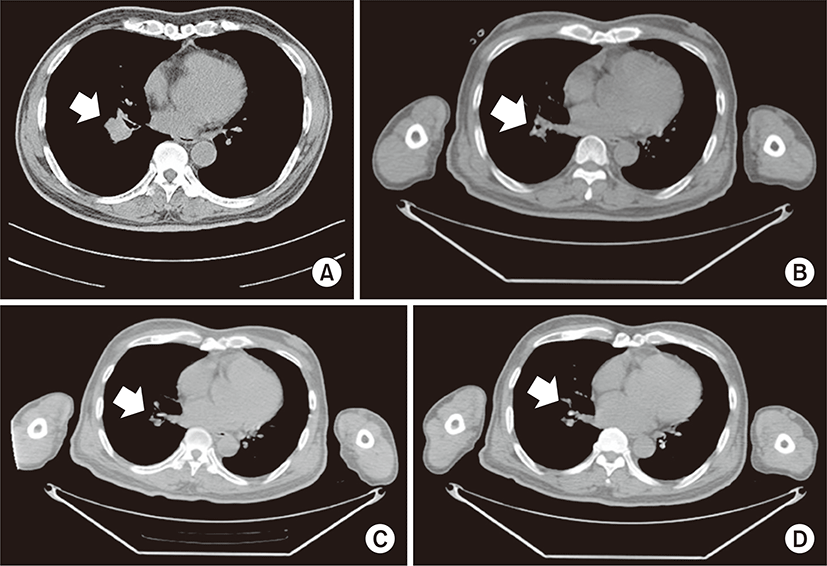
두 번째 항암 주기를 위해 외래 방문 시 2도 호중구 감소증(absolute neutrophil count [ANC] 1,393/μL)소견이 확인되어, 1주일 연기하여 항암제를 투여하였다. 세 번째 항암 주기는 특별한 연기 없이 진행 되었으나, 8일에 계획한 항암제 투여는 3도 호중구 감소증(ANC 652/μL)으로 투여하지 못하였다. 15일과 22일에도 호중구 감소증이 호전되지 않아, 추가 항암제 투여 없이 세 번째 주기를 종료하였다. 이후 시행한 PET 스캔에서는, 이전 검사에서 관찰되었던 종괴의 크기와 fluorodeoxyglucose (FDG) 섭취 증가 소견이 감소한 것으로 확인되었다(Fig. 1B).
부분 관해 소견이 확인된 상태에서 네 번째 항암 주기를 시작하였고, 8일 방문 시 2도 호중구 감소증(ANC 1,461/μL) 소견이 확인되어 항암제 투여를 1주일 연기하여 진행하였다. 지속적으로 8일에 호중구 감소증이 확인되는 바, 다섯 번째 항암 주기부터는 4주 간격으로 1일, 15일에 화학요법 진행하기로 하였고, 이 일정에 따라 다섯 번째와 여섯 번째 항암 주기는 연기 없이 진행되었다.
여섯 번째 항암 주기 이후 PET 스캔 검사를 시행하였고, 이전에 관찰되었던 FDG 섭취 증가 소견은 관찰되지 않아 대사적 측면에서 완전 관해로 판단, 화학요법 중단 후 경과 관찰 하기로 하였다(Fig. 1C). 6주 이후 PET 스캔으로 추적 검사를 진행하였고, 역시 악성을 시사하는 소견이 관찰되지 않아(Fig. 1D) 화학요법 없이 외래에서 추적 관찰 하던 중 추적 관찰 종료 하였다.
73세 남자가 경도의 호흡곤란을 주소로 내원하였다. 환자는 25갑년의 흡연력이 있었으며, 고혈압 및 당뇨로 경구 약제를 복용 중이었고, 3년 전 통풍으로 치료 받았던 과거력이 있었다. 환자는 9개월 전부터 발생한 우측 손목의 통증 및 호흡 곤란을 주소로 연고지 근처 병원을 방문하였고, 우측 손목관절 흡인 검사에서 통풍성 관절염이 진단되었다. 이때 시행한 흉부 단순촬영에서 좌하엽의 폐렴 소견이 보여 항생제 치료를 하였으나 호전이 없었고, 이에 CT 및 기관지 내시경을 시행한 결과 좌하엽에 위치한 악성 종괴 및 이와 동반된 폐쇄성 폐렴이 의심되어 본원으로 의뢰되었다.
내원 시 활력 징후와 신체 검진에서 특이 사항은 없었다. 혈액검사에서 백혈구 16,470/μL, 혈색소 13.4 g/dL, 혈소판 344,000/μL로 확인되었고, 일반 화학 검사에서 Na/K/Cl 130/5.4/94 mmol/L, Ca/P 9.7/4.0 mg/dL, BUN/Cr 102/3.8 mg/dL, AST /ALT 12/12 IU/L, total bilirubin 0.6 mg/dL, ALP 122 IU/L, uric acid 8.7 mg/dL였다.
흉부 단순촬영에서 좌하엽 부위에 미세한 음영변화가 관찰되었으며, 흉부 CT검사에서 좌하엽의 종괴, 종격동의 7번 림프절 종대, 좌측 쇄골상 림프절 종대, 간 전이 의심 소견이 확인되었다. 뇌 자기공명영상 (magnetic resonance imaging, MRI)에서 원격 전이는 관찰되지 않았고, 전신 PET 스캔에서 좌측 폐문부 림프절, 좌측 쇄골상 림프절, 그리고 간 전이 의심 부위의 FDG 섭취 증가소견이 확인되었다. 기관지 내시경 하 생검에서 소세포 폐암이 확인되었다.
내원 당시 혈액 검사에서 BUN/Cr 상승 소견이 관찰되었고, 원인 감별을 위한 신장 초음파 검사를 시행하였다. 검사 결과, 양측 신장에서 신피질의 초음파 음영 증가, 신실질의 혈류 감소 소견이 확인되었고, 이는 만성 콩팥병에 합당한 소견이었다. 당뇨병과 고혈압에 의한 만성 신부전으로 판단, 혈액투석도관 삽입 후 주 3회 일정으로 투석을 시작하였다.
확장기 소세포 폐암으로 진단, carboplatin (5 AUC, 1일)과 etoposide (50 mg/m2, 1일, 3일)를 3주 주기로 투여하는 화학요법을 시작하였다. 화학요법 당일에 항암제 주입이 끝난 후 혈액 투석을 시행하였고, 화학요법이 없는 날은 연고지에서 주 2회 또는 3회 투석치료를 지속하도록 하였다.
세 번째 항암 주기까지 특별한 부작용 없이 예정된 일정 대로 화학요법을 완료하였고, 이후 시행한 흉부 CT검사에서 부분 관해가 확인되어 화학요법을 지속하기로 하고 네 번째 항암 주기를 시작하였다. 22일에 다섯 번째 항암 주기를 위해 내원하였으나 2도 호중구 감소증(ANC 1,020/μL) 소견이 확인되어 항암제 투여를 1주일 연기 하였으며, 이후 6번째 항암 주기까지는 4주 간격으로 화학요법을 진행하였다.
여섯 번째 항암 주기 이후 시행한 흉부 CT 및 PET 스캔 검사 결과, 간 전이 병변의 진행 소견이 확인되었고, 이에 항암제를 cisplatin (20 mg/m2, D1, D8)과 irinotecan (50 mg/m2, 1일, 8일)으로 변경하여 투약하기로 하였다. 투석 일정은 이전과 같이 유지하였다.
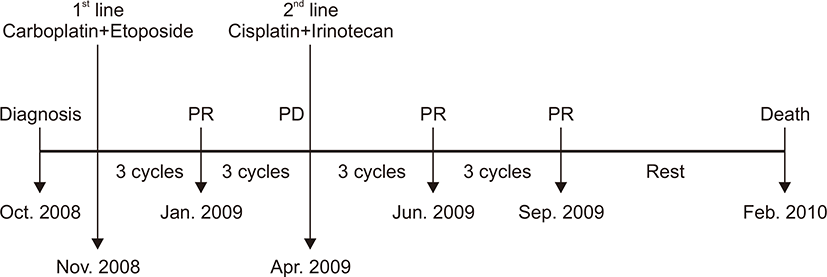
첫번째 주기 화학요법을 진행한 후, 발열, 기침, 가래 및 경도의 호흡곤란으로 입원하였고, 검사 결과 폐 결핵이 확인되어 이에 대한 약물치료를 시작하였으며, 항암제 투여는 2주일 후 재개하였다. 네 번째 항암 주기 중, 8일째 항암제 투여가 호중구 감소증으로 1주일 연기되었던 것 외에는 특별한 합병증 또는 항암제 투여 연기 없이 여섯 번째 항암 주기까지 치료를 완료 하였다. 이후 시행한 흉부 CT 검사에서 부분 관해 소견이 확인되었고, 이에 화학요법을 잠시 중단한 상태에서 경과 관찰 하기로 하였다. 추적 관찰 중, 치료 중단 3개월 경과 시점에 폐렴이 발생하여 내원하였고, 입원하여 항생제 치료 등을 시행하였으나, 다발성 장기부전으로 사망하였다(Fig. 2).
고 찰
국내의 투석 환자는 증가하는 추세에 있으며, Na 등[1]이 보고한 한국 자료에 따르면, 최근 만성 신부전 환자에서의 5년 누적 폐암, 유방암 발생이 증가하는 것으로 나타나고 있다. 소세포 폐암은 전체 폐암 환자의 18% 정도를 차지하며, 진단 시부터 대부분의 환자가 확장기 질환(extensive stage disease)로 진단된다. 확장기 소세포 폐암은 치료를 하지 않을 경우 생존기간이 2~3개월로 짧지만, 화학요법에 대한 반응률 또한 60~80%로 높아, 치료 시 생존기간이 8~13개월로 유의하게 증가함이 알려져 있다. 하지만 신기능 저하 환자에서는 적절한 항암제 용량에 대한 약동학적 연구가 많지 않아, 잠재적인 항암제 독성 증가의 위험으로 인해 적극적인 화학요법을 진행하는데 어려움이 있다.
소세포 폐암의 치료에는 항암제의 효과와 독성을 고려, platinum compounds를 바탕으로 한 조합이 표준적인 치료로 사용되며, cisplatin+etoposide가 대표적인 조합으로 사용된다. 한편, 이를 변형하여 cisplatin을 carboplatin으로 대체하거나, etoposide를 irinotecan으로 대체한 조합 역시 비슷한 효과를 가진 것으로 확인되어 현재 임상에서 사용되고 있다. 하지만 신기능 저하 환자에서 이들 항암제의 사용에 대해서는 체계적인 임상시험 연구가 없고 소수의 증례 보고만이 있는 실정이다[2-6].
소세포 폐암에서 사용되는 항암제 중, irinotecan의 경우, 주로 간에서 대사가 되는 것으로 알려져 있어, 신기능 저하 환자에서도 용량 조절 없이 사용할 수 있다. 하지만 platinum compounds의 경우, 신기능이 약물의 배출에 중요한 역할을 하는 것으로 알려져 있어, 신기능 저하 환자에서의 사용이 용이하지 않다. Etoposide 또한 대부분 간에서 대사가 되지만, 신장으로의 배출 역시 약물의 제거에 중요한 부분을 차지하는 것으로 알려져 있어 투여 용량의 조절이 필요하다.
Cisplatin의 경우 정맥 투여 후 빠르게 조직으로 확산되며, 높은 단백결합률을 보인다. 정상 신기능을 가진 환자에서, 투여 24시간 이내에 90% 이상이 신장을 통해 배출되는 것으로 알려져 있으나, 투석치료를 받는 환자의 경우, 높은 단백결합률로 인해 투석을 통한 약물제거가 용이하지 않다. 소세포 식도암이 진단된 투석 환자에서 cisplatin (80 mg/m2, 1일) + etoposide (100 mg/m2, 1일, 3일, 5일)로 투여하고 매 항암제 투여 후 혈액 투석을 진행하여, 정상 신기능을 가진 환자와 비교하여 유의한 항암제 독성 증가 없이 화학요법을 진행한 예가 보고된 적이 있다[7].
Carboplatin의 경우 투여 24시간 이내에 70%가 신장을 통해 배출되는 것으로 알려져 있어, 신기능 저하 환자에서 사용 시 독성이 증가할 위험이 있다. 신기능 저하 환자에서 목표 AUC를 유지하기 위한 carboplatin 용량을 계산하기 위해 Calvert formula를 사용하지만[8], 이는 사구체여과율이 33~135 mL/min인 환자를 대상으로 모은 자료를 바탕으로 개발된 것이라는 한계점이 있다. 하지만 최근 들어 투석 환자에게도 Calvert formula를 적용하여, 목표 AUC에 도달하기 위한 적정 용량을 계산하는 것이 가능 하다는 연구가 보고되고 있다[6].
Etoposide의 경우, 간의 CYP3A4, CYP3A5 경로를 통해 대사가 되기는 하지만, 신장을 통해 40% 정도가 배출되는 것으로 알려져 있다. 이러한 이유로 인해, 신기능 저하 환자에서 etoposide의 AUC가 유의하게 증가함이 확인되었고, 따라서 투석 환자에서는 표준 용량과 비교하여 용량을 50% 줄여 사용할 것이 권고되고 있다[9].
증례 1의 경우, carboplatin (5 AUC, 1일)과 irinotecan (50 mg/m2, 1일, 8일)을 3주 간격으로 투여하였다. 이전 연구에 사용된 항암제 용량은 carboplatin (5 AUC, 1일)과 irinotecan (50 mg/m2, 1일, 8일, 15일)를 4주 간격으로 투여하는 것이었으나[10], 이 증례의 경우 환자의 연령 및 전신상태를 고려하여 irinotecan의 용량을 33% 감량하였다. 첫 번째 항암 주기 이후 2도의 호중구 감소증으로 두 번째 항암 주기가 연기되었으나, 호중구 감소성 발열과 같은 심각한 합병증은 관찰되지 않았다. 또한 irinotecan에 의한 설사나 복통 같은 소화기계 부작용 역시 관찰되지 않았다. 반복되는 골수 억제 효과로 인해 네 번째 항암 주기부터는 carboplatin은 4주 간격으로, irinotecan은 2주 간격으로 투여하였으나, 결과적으로는 여섯 번째 항암 주기까지 항암제로 인한 심각한 합병증 없이 화학요법이 완료되었다.
증례 2의 경우 carboplatin(5 AUC, 1일)과 etoposide(50 mg/m2, 1일, 3일)를 3주 간격으로 투여하기로 하고 화학요법을 진행하였다. 일반적인 용량은 carboplatin(5 AUC, 1일)과 etoposide(100 mg/m2, 1~3일)이나, 환자의 연령, 전신상태 및 신기능을 고려하여 etoposide의 용량을 66% 감량하여 투여하였다. 네 번째 항암 주기까지 특별한 합병증 없이 지정된 일정대로 화학요법을 진행하였으나, 다섯 번째 주기부터는 2도 호중구 감소증으로 인해 4주 간격으로 화학요법을 진행하였다. 하지만, 여섯 번째 항암 주기까지 3도~4도에 해당하는 심각한 합병증 없이 항암제 투여를 완료하였다. 이후 시행한 검사에서 질병의 진행 소견이 확인되어 cisplatin (20 mg/m2, 1일, 8일)과 irinotecan (50 mg/m2, 1일, 8일)로 항암제를 변경하여 치료를 지속하였다. 이는 환자의 연령과 전신상태를 고려, 일반적으로 사용되는 cisplatin (30 mg/m2, 1일, 8일)과 irinotecan (65 mg/m2, 1일, 8일)에 비해 cisplatin은 33%, irinotecan은 23% 감량된 용량이었다. 이 경우 치료 기간 중 항암제로 인한 특별한 독성 또는 예정된 치료 주기의 지연 없이 여섯 번째 항암 주기까지 완료하였다. 이후 부분 관해 상태에서 추적 관찰 하던 중, 화학요법과 관련이 없는 것으로 판단되는 폐렴으로 사망하였다.
투석치료를 진행하는 환자에서 적절한 항암제 용량에 대해서는 현재까지 자료가 부족한 상태이다. 하지만 이번 증례를 통해, 만성 신부전이 동반된 소세포 폐암환자에서 적절한 투석치료 및 항암 투여 일정 조정을 통해 심각한 항암제 독성의 증가 없이 화학요법을 시행할 수 있음을 확인할 수 있었다.